诺贝尔奖官网截图

早在上世纪 70 年代,免疫学界便率先提出「抑制性 T 细胞(Suppressor T cells)」的概念。但受限于当时实验技术的落后,不同团队的研究结果始终无法统一,甚至相互矛盾 —— 到了上世纪 80 年代初,这一曾经被寄予厚望的概念,已近乎被整个领域彻底废弃。
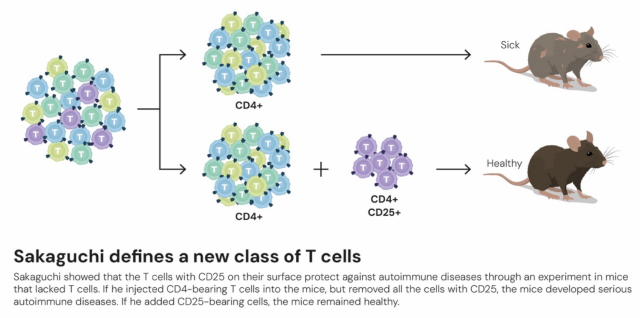
坂口志文定义了一种新的 T 细胞
进入 2001 至 2003 年,Brunkow 与 Ramsdell 的研究相继跟进,首次在分子层面清晰证实了 Treg 的客观存在与具体作用机制。至此,Treg 不再是一个模糊的「现象观察」,而是转变为有明确分子依据的「机制阐释」,研究基础被彻底夯实。
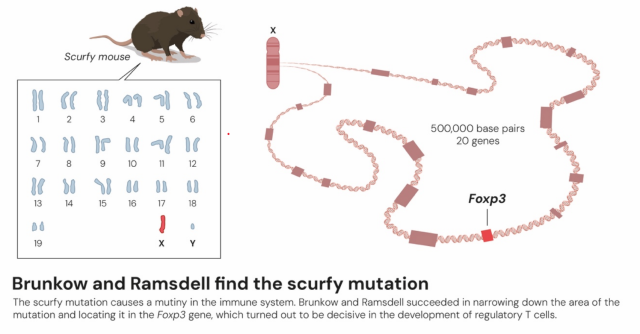
Brunkow 与 Ramsdell 发现了 scurfy 突变
只是,对于这样一个「起死回生」的科学概念而言,要让整个科学界打破固有认知、重新建立信任,最终全面接纳它,注定需要一段漫长的时间。

The body’s powerful immune system must be regulated, or it may attack our own organs. Mary E. Brunkow, Fred Ramsdell and Shimon Sakaguchi are awarded the Nobel Prize in Physiology or Medicine 2025 for their groundbreaking discoveries concerning peripheral immune tolerance that prevents the immune system from harming the body.
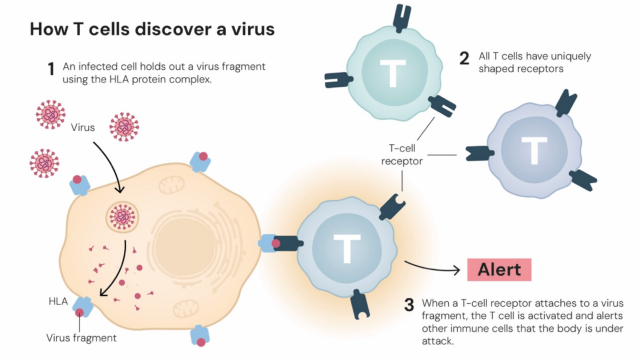
Every day, our immune system protects us from thousands of different microbes trying to invade our bodies. These all have different appearances, and many have developed similarities with human cells as a form of camouflage. So how does the immune system determine what it should attack and what it should defend?
Mary Brunkow, Fred Ramsdell and Shimon Sakaguchi are awarded the Nobel Prize in Physiology or Medicine 2025 for their fundamental discoveries relating to peripheral immune tolerance. The laureates identified the immune system’s security guards, regulatory T cells, which prevent immune cells from attacking our own body.
“Their discoveries have been decisive for our understanding of how the immune system functions and why we do not all develop serious autoimmune diseases,” says Olle Kämpe, chair of the Nobel Committee.
Shimon Sakaguchi was swimming against the tide in 1995, when he made the first key discovery. At the time, many researchers were convinced that immune tolerance only developed due to potentially harmful immune cells being eliminated in the thymus, through a process called central tolerance. Sakaguchi showed that the immune system is more complex and discovered a previously unknown class of immune cells, which protect the body from autoimmune diseases.
Mary Brunkow and Fred Ramsdell made the other key discovery in 2001, when they presented the explanation for why a specific mouse strain was particularly vulnerable to autoimmune diseases. They had discovered that the mice have a mutation in a gene that they named Foxp3. They also showed that mutations in the human equivalent of this gene cause a serious autoimmune disease, IPEX.
Two years after this, Shimon Sakaguchi was able to link these discoveries. He proved that the Foxp3 gene governs the development of the cells he identified in 1995. These cells, now known as regulatory T cells, monitor other immune cells and ensure that our immune system tolerates our own tissues.
The laureates’ discoveries launched the field of peripheral tolerance, spurring the development of medical treatments for cancer and autoimmune diseases. This may also lead to more successful transplantations. Several of these treatments are now undergoing clinical trials.

2025年诺贝尔生理学或医学奖揭晓
诺贝尔委员会主席奥勒・坎佩(Olle Kämpe)表示:“他们的发现对我们理解免疫系统的运作机制,以及为何并非所有人都会患上严重的自身免疫性疾病,起到了决定性作用。”
1995 年,下田章做出了首个关键发现,当时他的观点与主流认知相悖。在那个年代,许多研究者坚信,免疫耐受的形成仅仅是因为具有潜在危害性的免疫细胞在胸腺中通过一种名为 “中枢耐受” 的过程被清除。而下田章则证明,免疫系统的机制更为复杂,他还发现了一类此前未知的免疫细胞 —— 这类细胞能保护人体免受自身免疫性疾病的侵害。
2001 年,玛丽・布伦科和弗雷德・拉姆斯德尔取得了另一项关键突破:他们揭示了某一特定品系小鼠为何极易患上自身免疫性疾病。研究发现,这类小鼠体内存在一个基因突变,他们将该基因命名为Foxp3。此外,两人还证实,人类体内与该基因对应的基因若发生突变,会引发一种严重的自身免疫性疾病 ——IPEX 综合征(免疫失调、多内分泌腺病、肠病、X 连锁综合征)。
两年后,下田章成功将这些发现关联起来。他证实,Foxp3基因调控着他在 1995 年发现的那类细胞的发育。如今,这类细胞被称为 “调节性 T 细胞”,它们会监控其他免疫细胞,确保免疫系统对人体自身组织保持 “耐受”。
三位获奖者的发现开创了 “外周耐受” 这一研究领域,推动了癌症和自身免疫性疾病相关疗法的研发,也有望提高器官移植的成功率。目前,已有多项基于这些发现的疗法进入了临床试验阶段。





2024年–美国科学家Victor Ambros和Gary Ruvkun获奖,以表彰他们“发现microRNA及其在转录后基因调控中的作用”。
2023年——美国科学家Katalin Karikó和Drew Weissman获奖,获奖理由是“发现核苷基修饰,开发出了有效的对抗COVID-19的mRNA疫苗”。
2022年——瑞典科学家Svante Pääbo获奖,获奖理由是“在已灭绝古人类基因组和人类进化方面的发现”。
2021年——美国科学家David Julius、Ardem Patapoutian获奖,获奖理由是“发现温度和触觉的受体”。
2020年——美英三位科学家Harvey J. Alter、Michael Houghton和Charles M. Rice获奖,获奖理由是“发现丙型肝炎病毒”。
2019年——美英三位科学家William G. Kaelin Jr、Sir Peter J. Ratcliffe和Gregg L. Semenza获奖,获奖理由是“发现了细胞如何感知和适应氧气的可用性”。
2018年——美国科学家James P. Allision和日本科学家Tasuku Honjo获奖,获奖理由是“发现了抑制负面免疫调节的癌症疗法”。
2017年——三位美国科学家Jeffrey C. Hall、Michael Rosbash和Michael W. Young获奖,获奖理由是“发现了调控昼夜节律的分子机制”。
2016年——日本科学家Yoshinori Ohsumi获奖,获奖理由是“发现了细胞自噬机制”。
2015年——中国科学家屠呦呦获奖,获奖理由是“有关疟疾新疗法的发现”;另外两位获奖科学家为爱尔兰的William C. Campbell和日本的Satoshi ōmura,获奖理由是“有关蛔虫寄生虫感染新疗法的发现”。


近十年来,诺贝尔生理学或医学奖呈现多样化趋势,涵盖各个子学科,包括细胞生物学、免疫学、遗传学等。其中,基础研究占多数,也有重大临床成果获奖。在诺贝尔生理学或医学奖的发展历史中,诸多研究深刻影响了临床医学的实践,为人类攻克疾病开辟了全新的道路。

最年轻的获奖者是加拿大科学家弗雷德里克·班廷(Frederick G. Banting),1923年因“发现胰岛素”获奖,时年32岁。
最年长的获奖者是美国科学家佩顿·劳斯(Peyton Rous),1966年因“发现肿瘤诱导病毒”获奖,时年87岁。
获诺贝尔生理学或医学奖的华人科学家